Leczenie HER2 zależnego zaawansowanego raka piersi*

*Obwieszczenie Ministra Zdrowia z dnia 17 września 2025 r. w sprawie wykazu refundowanych leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych na 1 października 2025 r.

Lek objęty refundacją
w leczeniu przerzutowego lub
miejscowo zaawansowanego
raka piersi HER2-low
w leczeniu przerzutowego lub
miejscowo zaawansowanego
raka piersi HER2-low
OD 1 LIPCA 2025 ROKU
STRONA GŁÓWNA
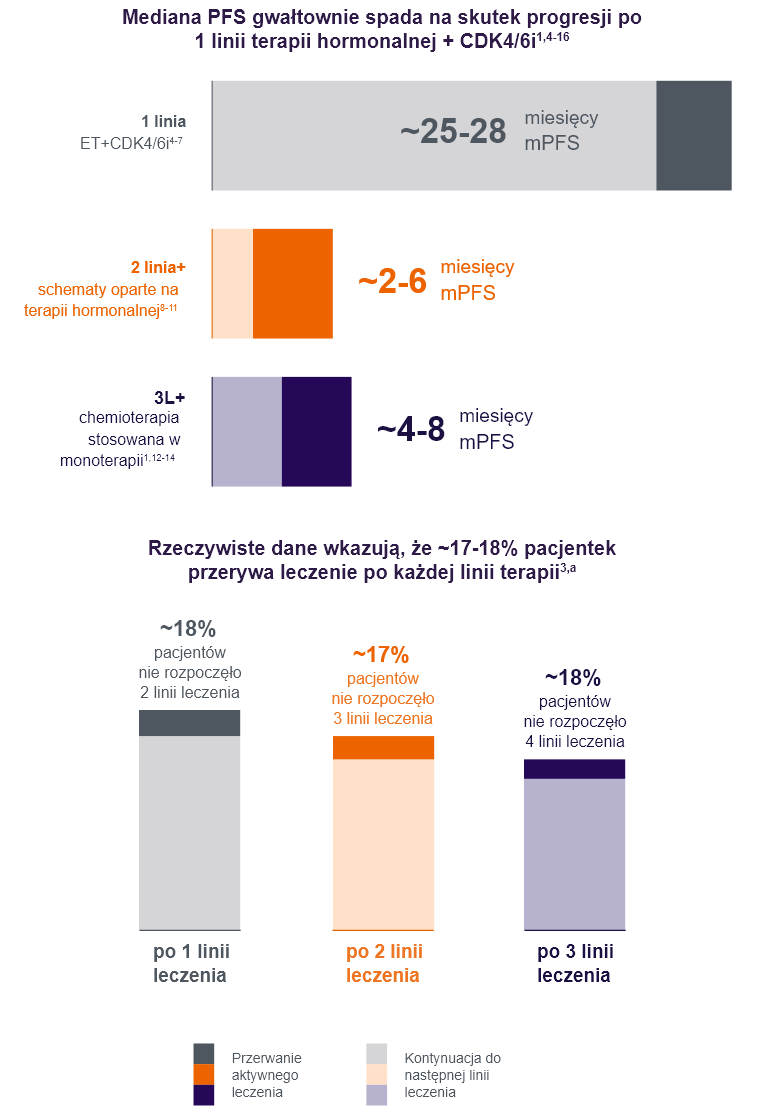
U pacjentek z przerzutowym rakiem piersi HR+/HER2- po 1L terapii hormonalnej w skojarzeniu z CDK4/6i, wyniki pogarszają się oraz zmniejsza się liczba pacjentek kontynuujących leczenie2,3
HER2-low istotną cechą kliniczną w raku piersi
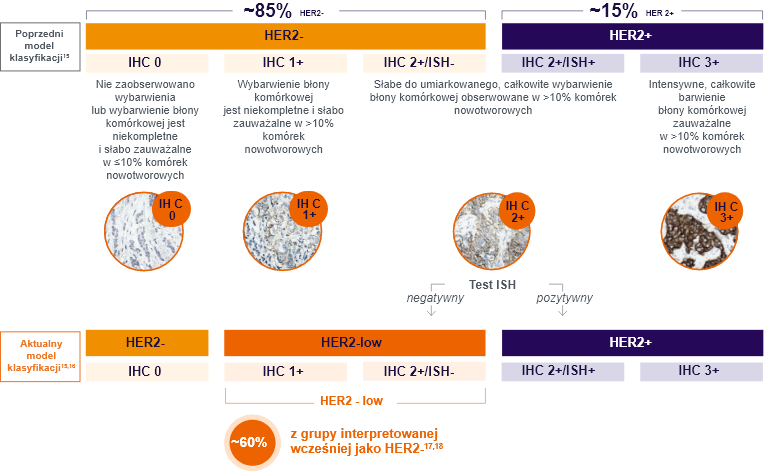
Pacjenci z rakiem piersi z wynikiem IHC 1+ lub IHC 2+/ISH- uznawani wcześniej jako HER2-, są obecnie klasyfikowani jako HER2-low.1,2
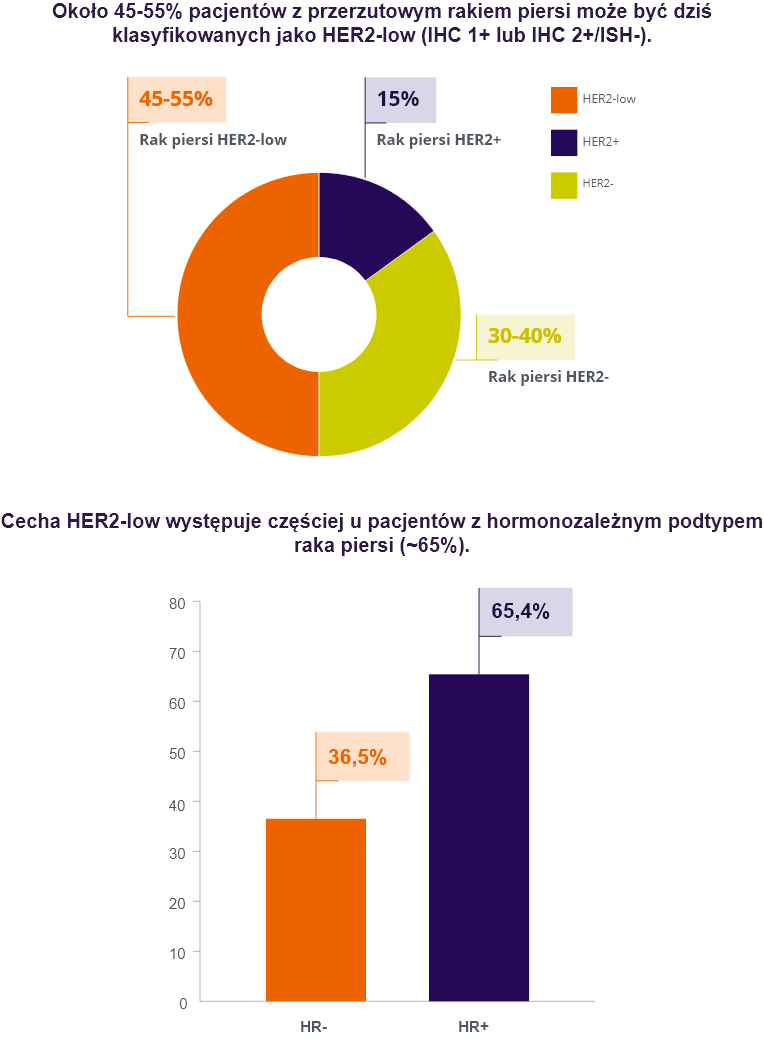
Wyróżnienie cechy HER2low otwiera nowe możliwości terapeutyczne dla wielu pacjentów z przerzutowym rakiem piersi.
Na podstawie danych z prowadzonego w Niemczech prospektywnego rejestru dotyczącego raka piersi, którego celem jest ocena schematów leczenia i jakości życia. W okresie od lipca 2014 r. do listopada 2022 r. do udziału w badaniu włączono 5012 pacjentek, w tym 2106 pacjentek z przerzutowym rakiem piersi HR+/HER2- podczas pierwszej linii leczenia, 1481 pacjentek podczas drugiej linii leczenia i 1077 pacjentek podczas trzeciej linii leczenia. Prosty wskaźnik rezygnacji obliczono na podstawie odsetka pacjentek, które ukończyły leczenie, ale nie rozpoczęły kolejnej linii leczenia.
1. ENHERTU [Draft Company Core Data Sheet]. Daiichi Sankyo Inc., Basking Ridge, NJ and AstraZeneca Pharmaceuticals LP, Wilmington, DE, 2024 2. Jhaveri K, Marmé F. Current and emerging treatment approaches for hormone receptor-positive/human epidermal growth factor receptor 2-negative metastatic breast cancer. Cancer Treat Rev. 2024;123:102670. doi:10.1016/j.ctrv.2023.102670 3. Hartkopf AD, Walter CB, Kolberg HC, i wsp. Attrition in the first three therapy lines in patients with advanced breast cancer in the german real-world PRAEGNANT registry. GebFra Science. 2024; 84(5):459-469 4. Finn RS, Martin M, Rugo HS, i wsp. Palbociclib and letrozole in advanced breast cancer. N Engl J Med. 2016;375(20):1925-1936. 5. Hortobagyi GN, Stemmer SM, Burris HA, I wsp. Updated results from MONALEESA-2, a phase III trial of first-line ribociclib plus letrozole versus placebo plus letrozole in hormone receptor-positive, HER2-negative advanced breast cancer. Ann Oncol. 2018;29(7):1541-1547. 6. Gennari A, André F, Barrios CH, i wsp. ESMO clinical practice guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Ann Oncol. 2021;32(12):1475-1495. 7. Johnston S, Martin M, Di Leo A, I wsp. MONARCH 3 final PFS: a randomized study of abemaciclib as initial therapy for advanced breast cancer. NPJ Breast Cancer. 2019;5:5. doi:10.1038/s41523-018-0097-z 8. Bidard FC, Kaklamani VG, Neven P, i wsp. Elacestrant (oral selective estrogen receptor degrader) versus standard endocrine therapy for estrogen receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: results from the randomized phase III EMERALD trial. J Clin Oncol. 2022;40(28):3246-3256. doi:10.1200/JCO.22.00338. Epub May 18, 2022. Erratum in: J Clin Oncol. 2023;41(23):3962. doi:10.1200/JCO.23.01239 9. Kalinsky K, Bianchini G, Hamilton EP, i wsp. Abemaciclib plus fulvestrant vs fulvestrant alone for HR+, HER2– advanced breast cancer following progression on prior CDK4/6 inhibitor plus endocrine therapy: primary outcome of the Phase 3 postMONARCH trial. Presented at: American Society for Clinical Oncology; May 31-June 4, 2024; Chicago, IL. 10. Rugo HS, Lerebours F, Ciruelos E, i wsp. Alpelisib plus fulvestrant in PIK3CA-mutated, hormone receptor-positive advanced breast cancer after a CDK4/6 inhibitor (BYLieve): one cohort of a phase 2, multicentre, open-label, non-comparative study. Lancet Oncol. 2021;22(4):489-498. doi:10.1016/S1470-2045(21)00034-6. Erratum in: Lancet Oncol. 2021;22(5):e184. doi:10.1016/S1470-2045(21)00194-7 11. Turner NC, Oliveira M, Howell SJ, i wsp. Capivasertib in hormone receptor–positive advanced breast cancer. N Engl J Med. 2023;388(25):2058-2070. 12. Bardia A, Jhaveri K, Im SA, i wsp. Datopotamab deruxtecan (Dato-DXd) vs chemotherapy in previously-treated inoperable or metastatic hormone receptor-positive, HER2-negative (HR+/HER2–) breast cancer: primary results from the randomised phase 3 TROPION-Breast01 trial. Presented at: European Society for Clinical Oncology; October 20-24, 2023; Madrid, Spain. 13. O’Shaughnessy J, Schwartzberg L, Piccart M, I wsp. Results from CONTESSA: a phase 3 study of tesetaxel plus a reduced dose of capecitabine versus capecitabine alone in patients with HER2-, hormone receptor + (HR+) metastatic breast cancer (MBC) who have previously received a taxane. Presented at: San Antonio Breast Cancer Symposium; December 8-11, 2020; San Antonio, TX. 14. Rugo HS, Bardia A, Marmé F, I wsp. Sacituzumab govitecan in hormone receptor-positive/human epidermal growth factor receptor 2-negative metastatic breast cancer. J Clin Oncol. 2022;40(29):3365-3376. 15. NCCN Clinical Practical Guidelines in Oncology, Breast Cancer. Version 6.2024, November 11, 2024, NCCN.org 16. Marszałek A., Krzakowski M., Onkologia w Praktyce Klinicznej — EDUKACJA ISBN 978-83-67879-55-2, Zalecenia dotyczące oceny czynnika predykcyjnego HER2 u chorych z rozpoznaniem inwazyjnego (naciekającego) raka piersi — aktualizacja na rok 2023. Stanowisko Konsultantów Krajowych w dziedzinie patomorfologii I onkologii klinicznej, 2023. 17. Tarantino P, Hamilton E, Tolaney SM, I wsp. HER2-low breast cancer: pathological and clinical landscape. J Clin Oncol. 2020;38(17):1951-1962. 18. Schettini F, Chic N, Brasó-Maristany F, I wsp. Clinical, pathological, and PAM50 gene expression features of HER2-low breast cancer. NPJ Breast Cancer. 2021;7(1):1-13 19. Tarantino P, Hamilton E, Tolaney SM, I wsp. HER2-low breast cancer: pathological and clinical landscape. J Clin Oncol. 2020;38(17):1951-1962. 20. Schettini F, Chic N, Brasó-Maristany F, I wsp. Clinical, pathological, and PAM50 gene expression features of HER2-low breast cancer. NPJ Breast Cancer. 2021;7(1):1-13. 21. Paolo Tarantino, MD, I wsp. HER2-Low Breast Cancer: Pathological and Clinical Landscape, https://ascopubs.org/doi/10.1200/JCO.19.02488
1. ENHERTU [Draft Company Core Data Sheet]. Daiichi Sankyo Inc., Basking Ridge, NJ and AstraZeneca Pharmaceuticals LP, Wilmington, DE, 2024 2. Jhaveri K, Marmé F. Current and emerging treatment approaches for hormone receptor-positive/human epidermal growth factor receptor 2-negative metastatic breast cancer. Cancer Treat Rev. 2024;123:102670. doi:10.1016/j.ctrv.2023.102670 3. Hartkopf AD, Walter CB, Kolberg HC, i wsp. Attrition in the first three therapy lines in patients with advanced breast cancer in the german real-world PRAEGNANT registry. GebFra Science. 2024; 84(5):459-469 4. Finn RS, Martin M, Rugo HS, i wsp. Palbociclib and letrozole in advanced breast cancer. N Engl J Med. 2016;375(20):1925-1936. 5. Hortobagyi GN, Stemmer SM, Burris HA, I wsp. Updated results from MONALEESA-2, a phase III trial of first-line ribociclib plus letrozole versus placebo plus letrozole in hormone receptor-positive, HER2-negative advanced breast cancer. Ann Oncol. 2018;29(7):1541-1547. 6. Gennari A, André F, Barrios CH, i wsp. ESMO clinical practice guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Ann Oncol. 2021;32(12):1475-1495. 7. Johnston S, Martin M, Di Leo A, I wsp. MONARCH 3 final PFS: a randomized study of abemaciclib as initial therapy for advanced breast cancer. NPJ Breast Cancer. 2019;5:5. doi:10.1038/s41523-018-0097-z 8. Bidard FC, Kaklamani VG, Neven P, i wsp. Elacestrant (oral selective estrogen receptor degrader) versus standard endocrine therapy for estrogen receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: results from the randomized phase III EMERALD trial. J Clin Oncol. 2022;40(28):3246-3256. doi:10.1200/JCO.22.00338. Epub May 18, 2022. Erratum in: J Clin Oncol. 2023;41(23):3962. doi:10.1200/JCO.23.01239 9. Kalinsky K, Bianchini G, Hamilton EP, i wsp. Abemaciclib plus fulvestrant vs fulvestrant alone for HR+, HER2– advanced breast cancer following progression on prior CDK4/6 inhibitor plus endocrine therapy: primary outcome of the Phase 3 postMONARCH trial. Presented at: American Society for Clinical Oncology; May 31-June 4, 2024; Chicago, IL. 10. Rugo HS, Lerebours F, Ciruelos E, i wsp. Alpelisib plus fulvestrant in PIK3CA-mutated, hormone receptor-positive advanced breast cancer after a CDK4/6 inhibitor (BYLieve): one cohort of a phase 2, multicentre, open-label, non-comparative study. Lancet Oncol. 2021;22(4):489-498. doi:10.1016/S1470-2045(21)00034-6. Erratum in: Lancet Oncol. 2021;22(5):e184. doi:10.1016/S1470-2045(21)00194-7 11. Turner NC, Oliveira M, Howell SJ, i wsp. Capivasertib in hormone receptor–positive advanced breast cancer. N Engl J Med. 2023;388(25):2058-2070. 12. Bardia A, Jhaveri K, Im SA, i wsp. Datopotamab deruxtecan (Dato-DXd) vs chemotherapy in previously-treated inoperable or metastatic hormone receptor-positive, HER2-negative (HR+/HER2–) breast cancer: primary results from the randomised phase 3 TROPION-Breast01 trial. Presented at: European Society for Clinical Oncology; October 20-24, 2023; Madrid, Spain. 13. O’Shaughnessy J, Schwartzberg L, Piccart M, I wsp. Results from CONTESSA: a phase 3 study of tesetaxel plus a reduced dose of capecitabine versus capecitabine alone in patients with HER2-, hormone receptor + (HR+) metastatic breast cancer (MBC) who have previously received a taxane. Presented at: San Antonio Breast Cancer Symposium; December 8-11, 2020; San Antonio, TX. 14. Rugo HS, Bardia A, Marmé F, I wsp. Sacituzumab govitecan in hormone receptor-positive/human epidermal growth factor receptor 2-negative metastatic breast cancer. J Clin Oncol. 2022;40(29):3365-3376. 15. NCCN Clinical Practical Guidelines in Oncology, Breast Cancer. Version 6.2024, November 11, 2024, NCCN.org 16. Marszałek A., Krzakowski M., Onkologia w Praktyce Klinicznej — EDUKACJA ISBN 978-83-67879-55-2, Zalecenia dotyczące oceny czynnika predykcyjnego HER2 u chorych z rozpoznaniem inwazyjnego (naciekającego) raka piersi — aktualizacja na rok 2023. Stanowisko Konsultantów Krajowych w dziedzinie patomorfologii I onkologii klinicznej, 2023. 17. Tarantino P, Hamilton E, Tolaney SM, I wsp. HER2-low breast cancer: pathological and clinical landscape. J Clin Oncol. 2020;38(17):1951-1962. 18. Schettini F, Chic N, Brasó-Maristany F, I wsp. Clinical, pathological, and PAM50 gene expression features of HER2-low breast cancer. NPJ Breast Cancer. 2021;7(1):1-13 19. Tarantino P, Hamilton E, Tolaney SM, I wsp. HER2-low breast cancer: pathological and clinical landscape. J Clin Oncol. 2020;38(17):1951-1962. 20. Schettini F, Chic N, Brasó-Maristany F, I wsp. Clinical, pathological, and PAM50 gene expression features of HER2-low breast cancer. NPJ Breast Cancer. 2021;7(1):1-13. 21. Paolo Tarantino, MD, I wsp. HER2-Low Breast Cancer: Pathological and Clinical Landscape, https://ascopubs.org/doi/10.1200/JCO.19.02488